重磅 | 全球首款双报双批实体瘤CAR-T进入二期试验,百吉生物一期数据首次震撼亮相ESMO年会
作为肿瘤领域最具影响力的年度盛会之一2024年欧洲肿瘤内科学会(ESMO)年会2024年9月13-17日于西班牙巴塞罗那正式召开,本届年会云集全球顶尖的肿瘤专家与学者、汇聚领域最新进展,为来自世界各地的肿瘤学者和医疗人员提供高质量的教育和交流机会。
百吉生物,一家专注免疫细胞治疗具有国际竞争力的创新药公司,在本次ESMO年会展示了其自主研发的全球首创靶向EB病毒抗原治疗鼻咽癌的部分I期注册临床数据。
百吉生物目前已取得10个中美双报双批临床批文,均为全球首创第四代肿瘤产品,针对实体瘤,目前最快管线BRG01产品已处于II期临床试验阶段,另外两款全球首创产品管线BST02和BRL03的I期临床试验首例受试者均已入组,预计将在今年完成I期临床。

(从左到右:中山大学肿瘤防治中心肿瘤学博士,临床试验中心I期病房副主任医师 马宇翔副主任医师;中山大学肿瘤防治中心I期病房主任,临床研究部副主任 赵洪云教授; 百吉生物医药高级研发科学家 Dr. Statham Liu)

摘要名称
靶向EB病毒包膜糖蛋白的新型CAR-T细胞疗法(BRG01)在晚期转移性鼻咽癌(NPC)患者中的安全性和有效性
摘要编号
899P
此次展示指出,BRG01的Ⅰ期注册临床已经顺利完成DLT(剂量限制性毒性)观察和9例患者的疗效评估,受试者均为晚期鼻咽癌患者,100%的受试者经历过铂类化疗治疗以及至少一种包括PD-1抗体等免疫检查点抑制剂治疗失败,且45%的受试者经过抗体偶联ADC临床试验药物治疗失败。
数据显示,BRG01展现出了卓越的安全性和有效性:安全性方面,接受治疗的患者均没有出现剂量限制性毒性,神经毒性,2级以上细胞因子风暴以及治疗相关死亡事件,其中≥3级的不良事件多为清淋方案带来的短暂性白细胞降低。
有效性方面,疾病控制和疗效呈现明显的剂量相关性。疗效在中高剂量中更为显著,其中75%患者出现持续肿瘤病灶缩小并代谢活性降低,少数患者甚至实现了肿瘤病灶100%持续完全缓解(CR)。
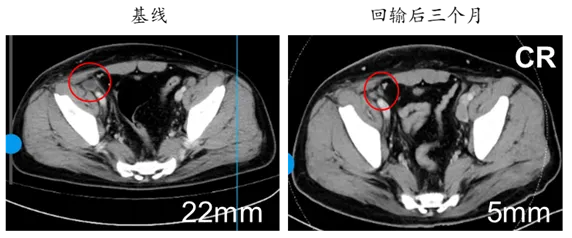
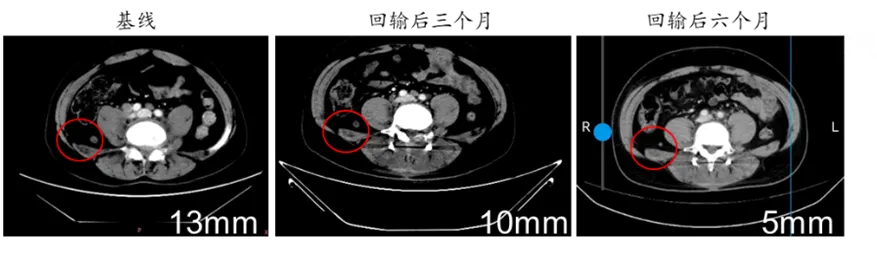
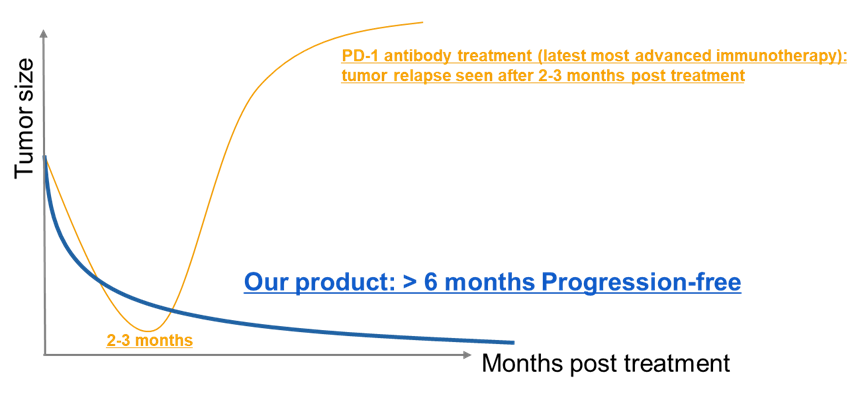
在疾病控制方面,BRG01回输后的患者可以持续无进展生存超过6个月,目前还在持续随访中,相比于现有最优的疗法PD1抗体,显示出显著延长的抗肿瘤效果以及患者的无进展生存期。
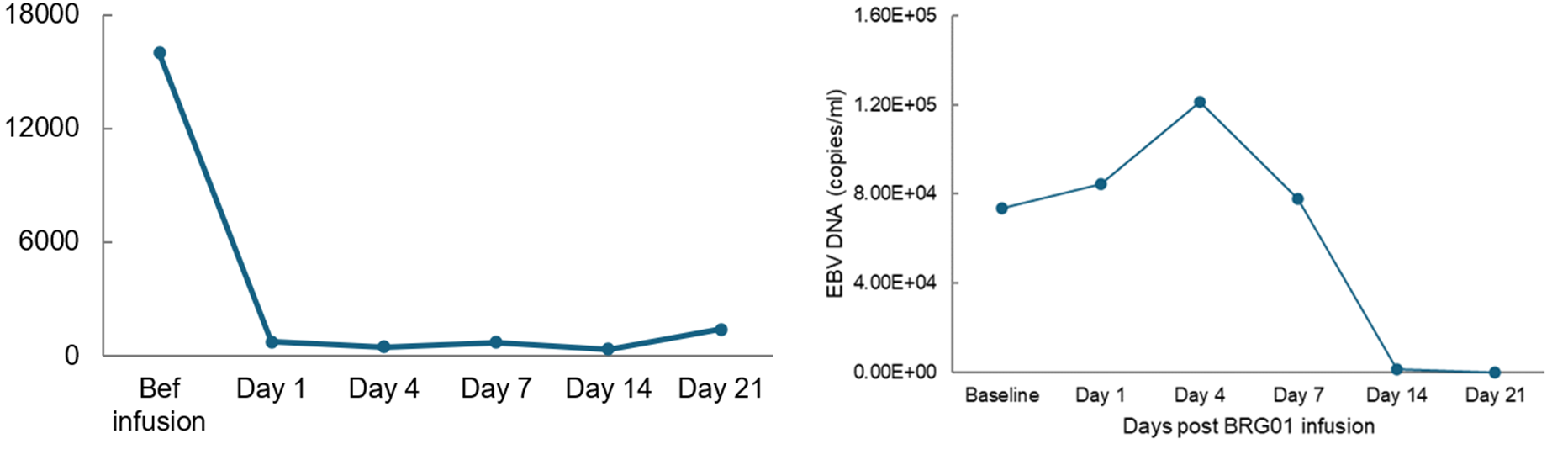
此外,BRG01还表现出卓越的抗EB病毒效力,患者回输后外周血中的EB病毒载量显著降低至正常水平。
此项临床试验的主要研究者(PI),中山大学肿瘤防治中心I期病房主任、中山大学肺癌研究所副主任张力教授指出:“BRG01是针对EBV阳性肿瘤的潜在‘first-in-class’ T细胞药物,其独特的机制和优秀的1期数据让我们对其在II期临床上的表现充满信心。我们期待通过进一步的临床研究,确立其良好的临床有效性,为更多患者带来治疗的新希望。”
据此前报道,BRG01 II期临床试验许可已分别于今年7月(中国)和8月(美国)获批,目前已经启动II期临床试验患者入组。
这些数据不仅彰显了BRG01在肿瘤治疗中的潜力,还表明其在抗病毒治疗方面的双重优势,为未来的临床应用奠定了坚实的基础,相信这也是CDE和FDA批准BRG01进入II期临床的重要依据。
BRG01是一款通过基因修饰技术,将靶向EB病毒(Epstein-Barr virus, EBV)抗原的嵌合受体表达于T细胞表面的自体T细胞免疫治疗产品,是百吉生物全球首创针对EBV特异性的新一代CAR-T细胞疗法。该疗法于2022年12月与2023年2月分别获得CDE和FDA的临床默示许可,随后在2023年6月、7月接连被FDA授予孤儿药ODD资格认定和快速通道FTD资格认定,中美双报进展势如破竹。
在今年5月召开的美国基因与细胞治疗年会(CSGCT)上,百吉生物展示了该疗法的临床前研究成果,相关数据还作为原创研究发表在Frontiers in Immunology上。此外,在今年6月初瑞士召开的鼻咽癌高登研究会议(GRC)上,百吉生物科学家兼管线发明人、德国科隆大学医学院转化免疫所主任、汉诺威医学院Renata Stripecke教授也展示了这一疗法的临床前研究成果和最新临床数据。
众所周知,细胞治疗药物在血液瘤领域已经取得瞩目成果,国内也已有5款针对血液系统肿瘤的CAR-T产品获批上市,但实体瘤领域还迟迟未能突破。今年2月,FDA加速批准了Iovance的TIL疗法lifileucel,用于晚期黑色素瘤治疗,开启了实体瘤细胞药物的商业化时代。这给众多正在开发实体瘤细胞疗法的企业带来了巨大的信心。然而,要攻克实体肿瘤确实不易,从一开始的技术、靶点和适应症选择,就需要有独到的眼光与视角,既要满足临床患者需求,又要充分考虑其可成药性。
就以鼻咽癌来看,这是一种发生于鼻咽部黏膜上皮的恶性肿瘤,是常见的头颈部恶性肿瘤之一。根据世界卫生组织数据显示,2020年全球确诊的鼻咽癌新发病例数达到13.3万人,中国鼻咽癌新发病例约占全球的50%,特别是广东及广西属于高发地区,约占全中国新发病例的60%。近年来免疫检查点抑制剂开始用于鼻咽癌的二线及以上治疗,总体反应率(ORR)均不高于30%,这意味着超过70%的患者不能从中获益,存在巨大的未被满足的临床需求。
而鼻咽癌的发生发展与EBV的感染密切相关。EBV在人群中的感染率超90%,已被世界卫生组织定义为I类致癌物,与其相关的肿瘤主要包括鼻咽癌、EBV阳性的胃癌、淋巴瘤和淋巴细胞增生性疾病等。研究发现,鼻咽癌肿瘤细胞常表达EBV抗原,而EBV阳性的肿瘤细胞则表达CD4+T细胞、CD8+T细胞的靶蛋白,这便十分有利于靶向EBV的CAR-T细胞浸润肿瘤组织并发挥杀伤功能。
百吉生物在实体瘤细胞治疗领域的布局远不止于此,目前,公司已成为同时拥有CAR-T、TCR-T和TIL等针对实体瘤和血液瘤的三大细胞疗法的biotech企业,并且相关产品管线均已完成中美双报双批,后两者的适应症涵盖肺癌、肝癌等多种实体肿瘤。
对于BRG01注射液I期临床数据的首次发布,百吉生物联合创始人兼首席执行官Dr. Michelle Chen表示:“BRG01注射液是我们团队多年努力的结果,也是对公司核心技术和研发实力的高度认可。百吉生物始终致力于全球首创原研新药的研发,以满足肿瘤治疗领域未被满足的临床需求。未来,我们将继续加大研发投入,加速推进BRG01的临床试验和上市进程,为全球患者提供更有效、更可及的治疗选择。”
在百吉生物的高效执行与快速研发成果下,我们有理由期待实体瘤细胞药物在更快更短的时间内实现更多的临床突破,为患者带来新的治疗希望。